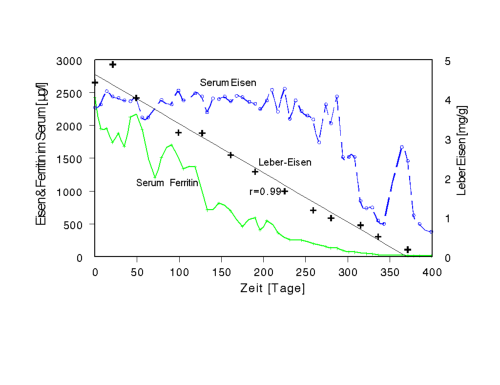
Abb1: Typischer Verlauf einer erschöpfenden Aderlasstherapie bei einem 40-jährigen Mann mit mittelschwerer
Eisenüberladung. Im Laufe eines Jahres wurden 52 Aderlässe durchgeführt. Darunter fällt das Lebereisen (hier
mit dem Biomagnetometer gemessen) linear ab. Das Ferritin fluktuiert zu anfang stark. Das Serum-Eisen bleibt
solange hoch, bis alles Speichereisen verbraucht wurde.
Es empfiehlt sich deshalb grundsätzlich das Blutabnehmen im Liegen. Schlechte Venenverhältnisse sind eher
selten ein wirkliches Hindernis. In Einzelfällen kann man auch z.B. mit „Butterfly“-Bestecken aus der Hand
größere Blutmengen abnehmen, ansonsten haben sich geschlossene Blutabnahmebestecke wie beim
Blutspenden sehr bewährt. Offene Systeme, oder Vakuumflaschen sind in der Praxis weniger gut geeignet.
Nach einer Therapiepause von ca. 3-6 Monaten wird dann nach Wiederanstieg der empfindlichen
Blutparameter (Serum-Fe, Transferrin-Fe-Sättigung) eine Erhaltungstherapie (3-6 Aderlässen/Jahr)
durchgeführt, um die weiter überschüssig aufgenommenen Eisenmengen gleich wieder zu entfernen und somit
einer Reakkumulation von Eisen dauerhaft entgegenzuwirken.
Die Aderlasstherapie ist einfach, sicher, effizient, kostengünstig und in fast allen Fällen als gut verträglich
bekannt. Bei bereits schwer kranken Patienten, die eine Aderlasstherapie anfangs nicht tolerieren, kann
alternativ sehr erfolgreich eine Therapie mit dem Eisenchelator Deferoxamin durchgeführt werden (Abb. 2.).
Aktuell wird auch der neue Eisenchelator Deferasirox (ExjadeR) in einer Studie an Patienten mit hered.
Hämochromatose getestet. Auch dies ist wirksam, wie eigenen Erfahrungen damit zeigen.
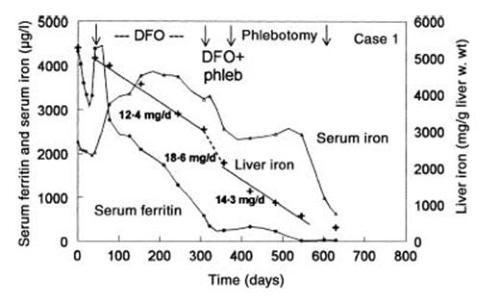
Abb. 2: Desferal®-Therapie bei hered. Hämochromatose in Fällen bei denen keine Aderlasstherapie möglich
ist (23). Gezeigt ist der Abfall von Lebereisen und Serum-Ferritin bei einem Patienten in Phasen mit DFO-
Therapie oder Aderlass. Die Zahlenangaben bedeuten entfernte Eisenmasse in mg/d unter der jeweiligen
Therapie. DFO=Deferoxamin (Nielsen et al. 2003).
Die unspezifischen Symptome wie Schwäche, Lethargie, sowie Hautpigmentierung sprechen gut auf die
Aderlasstherapie an. Auch erhöhte Leberindikatorenzyme normalisieren sich oft rasch unter der
Aderlasstherapie, als Zeichen dafür, dass eine noch nicht irreversibel geschädigte Leber sich schnell erholen
kann. Berichte, dass auch eine Leberzirrhose reversibel sein soll bei Hämochromatose sind allerdings kaum
glaubwürdig. Auch ein Diabetes mellitus, eine Arthropathie und auch Impotenz sind meist nicht reversibel,
allerdings ist in vielen Fällen mit einer Stabilisierung der Krankheitssymptome zu rechnen.
Liegt z.B. bereits eine Leberzirrhose bei Hämochromatose vor, so ist unter Aderlasstherapie diese
Organschädigung deutlich weniger progressiv als bei Leberzirrhosen anderer Ursache z.B. bei chronischem
Ethanolabusus.
Die Prognose bei unbehandelter hereditärer Hämochromatose mit vorliegenden schweren Organschäden
(Leberzirrhose, Diabetes) ist schlecht. In der Vor-Insulin-Ära starben die klinisch betroffenen Patienten meist
am diabetischen Koma (5). Weitere häufige Todesursachen waren früher Kardiomyopathie und hepatozelluläres
Karzinom. Durch die Einführung der Aderlasstherapie hat sich die Lebenserwartung der Patienten mit
Hämochromatose wesentlich verbessert (24,25). Zwei umfangreiche Studien zur Langzeitprognose von
Hämochromatosepatienten sind in der Literatur bekannt (19,25). Die Studie aus Düsseldorf wurde unlängst
aktualisiert (26). Aus den Ergebnissen ergibt sich, dass die Überlebensrate gegenüber einer Geschlechts- und
Altersangepassten Gruppe von Normalpersonen erniedrigt ist. Betrachtet man allerdings nur die Gruppe der
Patienten, die bei Diagnosestellung noch keine schweren Organschäden wie Leberzirrhose oder Diabetes
aufweisen, so ist deren Lebenserwartung im Vergleich zur Normalbevölkerung unbeeinflusst. Dies betrifft die
überwiegende Mehrzahl der heute neu diagnostizierten Patienten.
Der Nutzen einer „eisenarmen Ernährung“ bei Hämochromatose wird unterscheidlich bewertet. Eine
fleischarme Diät mit ständigem Teetrinken dürfte die Eisenaufnahme von pfanzlichem Eisen deutlich
vermindern. Jedoch ist die Wirksamkeit der Aderlasstherapie in jedem Fall deutlich höher einzuschätzen, so
dass eine Diätempfehlung nicht zwingend ist.
Die Prognose bei unbehandelter hereditärer Hämochromatose mit individuell vorliegenden schweren
Organschäden (Leberzirrhose, Diabetes) ist schlecht.
Einschränkend muss man heute allerdings sagen, dass möglicherweise nur ein relativ kleiner Teil der genetisch
betroffenen Probanden wirklich schwere Organschäden ausbildet. In der Vor-Insulin-Ära starben die klinisch
betroffenen Patienten meist am diabetischen Koma (Sheldon 1935). Weitere häufige Todesursachen waren
früher Kardiomyopathie und hepatozelluläres Karzinom. Durch die Einführung der Aderlasstherapie hat sich die
Lebenserwartung der Patienten mit Hämochromatose wesentlich verbessert (Finch und Finch 1966, Niederau
1985). Zwei umfangreiche Studien zur Langzeitprognose von Hämochromatosepatienten sind in der Literatur
bekannt (Niederau et al. 1985, Adams et al. 1991, 1997). Die Studie aus Düsseldorf wurde unlängst aktualisiert
(Niederau et al. 1996). Aus den Ergebnissen ergibt sich, dass die Überlebensrate von
Hämochromatosepatienten gegenüber einer Geschlechts- und Alters-angepassten Gruppe von
Normalpersonen erniedrigt ist.
Betrachtet man allerdings nur die Gruppe der Patienten, die bei Diagnosestellung noch keine schweren
Organschäden wie Leberzirrhose oder Diabetes aufweisen, so ist deren Lebenserwartung im Vergleich zur
Normalbevölkerung unbeeinflusst. Der heute diagnostizierte typische Hämochromatosepatient gehört in die
Gruppe mit geringer bis ganz fehlender Symptomatik. Hier ist die Aderlasstherapie als vorsorgliche Maßnahme
zu sehen, die die Ausbildung von schweren Organschäden sicher verhindert.
Wichtig ist in jedem Fall die Frühdiagnose!!
Literatur
Adams PC, Speechley M, Kertesz AE (1991). Long-term survival analysis in hereditary hemochromatosis. Gastroenterology
101: 368-372.
Adams PC, Deugnier Y, Moirand R, Brissot P (1997) The relationship between iron overload, clinical symptoms, and age in
410 patients with genetic hemochromatosis. Hepatology 25:162-166.
Finch SC , Finch CA (1955) Idiopathic hemochromatosis and iron storage disease. Medicine 34:381-430.
Niederau C, Fischer R, Sonnenberg A, Stremmel W, Trampisch HJ, Strohmeyer G (1985) Survival and causes of death in
cirrhotic and non-cirrhotic patients with primary haemochromatosis. N Engl J Med 313:1256-1262.
Niederau C, Fischer R, Pürschel A, Stremmel W, Häussinger D, Strohmeyer G (1996) Long-term survival in patients with
hereditary hemochromatosis. Gastroenterology 110: 1107-1119.
Niederau C, Strohmeyer G, Stremmel W (1994) Epidemiology, clinical spectrum, and prognosis of hemochromatosis. Adv
Exp Med Biol 356:293-302.
Niederau C, Niederau CM, Lange S, et al. (1998) Screening for hemochromatosis and iron deficiency in employees and
primary care patients in Western Germany. Ann Intern Med 128: 337-345.
Nielsen P, Fischer R, Buggisch P, Janka-Schaub G. Effective treatment of hereditary haemochromatosis with
desferrioxamine in selected cases. Brit J Haematol 2003; 123:952–953
Sheldon JH (1935) Haemochromatosis, Oxford University press, London

James Gillray um 1805, London, Victoria und Albert Museum (Bild
Victoria und Albert Museum (Bild Quelle Wikipedia)
Quelle Wikipedia)
 Victoria und Albert Museum (Bild
Victoria und Albert Museum (Bild Quelle Wikipedia)
Quelle Wikipedia)











© www.eiseninfo.de
Therapie Eisenüberladung
Auch wenn sich das auf den ersten Blick als Rückgriff
auf das Mittelalter anhört, die erschöpfende
Aderlasstherapie (ca. 500 ml Blutentzug=250 mg
Eisen/Woche) ist die effektivste, sicherste, wirksamste
und billigste Behandlungsmöglichkeit bei der
erblichen Eisenspeicherkrankheit. Es wird solange
therapiert, bis sich eine leichte Eisenmangelanämie (Hb
stabil < 11 g/dl) einstellt. Nach einer Therapiepause von
ca. 6-12 Monaten wird dann nach Wiederanstieg der
empfindlichen Blutparameter (Serum-Fe, Transferrin-Fe-
Sättigung) eine Erhaltungstherapie (3-6 Aderlässe/ Jahr)
durchgeführt, um die weiter überschüssig
aufgenommenen Eisenmengen gleich wieder zu
entfernen und somit einer Reakkumulation von Eisen
dauerhaft entgegenzuwirken. Die Aderlasstherapie ist
sehr wirksam, sicher und in fast allen Fällen als gut
verträglich bekannt.
.
Aderlasstherapie
Aderlasstherapie bei einer Patientin mit Typ1 Hämochromatose (Vorgehen wie bei Blutspende)