Erhöhtes Serum-Ferritin
(normal 35-235 µg/l)
•
hereditäre Hämochromatose Typ 1
•
sehr selten bei uns: hereditäre Hämochromatose Typ 2-4 (Werte von 300- ca. 5000 µg/l)
•
Transfusionsbedingte Hämosiderosen (Werte von 500 - ca. 10000 µg/l)
•
sehr selten: Hyperferritinämie-Katarakt-Syndrom (Werte ca. 1000 µg/l)
•
•
akute-Phase-Protein, auch als Tumormarker; sehr selten: Still disease
•
Freisetzung aus der Leber bei akuten Leberzellschäden (?, z.B. 500-3000 µg/l)
•
nutritiv bedingte Eisenüberladung (bei Übergewicht, Fettleber) (300-1000 µg/l)
•
Z.n. (nichtindizierter) oraler Eisentherapie (Werte bis ca. 500 µg/l)
•
Z.n. (nichtindizierter) i.v. Eisentherapie (Werte bis ca. 500 µg/l)
Bei exzessiv erhöhter Eisenspeicherung (Hämochromatosen, “iron-loading-anemias” und
Transfusionsbedingten Hämosiderosen) ist zeigt das Serum-Ferritin quasi richtig die Gegenregulation von
zellen an, das zuviel an Eisen in Form von Ferritin zu speichern. 
Das Hyperferritin-Katarakt-Syndrom (HHCS) ist eine autosomal dominant vererbte Erkrankung, die bei
Kindern und Erwachsenen zu einer isolierten Ferritin-Erhöhung führt, ohne daß eine deutlich erhöhte
Transferrinsättigung oder eine hepatische Eisenüberladung nachweisbar ist (1). Ursache ist eine
mutationsbedingte Überproduktion der L-Untereinheit des Ferritins. Diese L-Untereinheit kann in Geweben
quasi auskristallisieren, was sich an einer fortschreitenden beidseitigen Linsentrübung im Alter zwischen 4-40
Jahren bemerkbar machen kann.
Bei akuten und chronischen Infekten sowie bei Autoimmunerkrankungen wird ein im Vergleich zum
Speichereisen zu hohes Plasma-Ferritin bestimmt. Dies gilt ebenso bei Leukämien und Lymphomen durch
Eisenspeicherung in den Leukozyten sowie in Folge einer Freisetzung bei Erkrankungen mit Leberparenchym-
schädigungen (Hepatitis, toxische Leberschädigung, u.a.).
Nutritiv bedingte Eisenüberladung?
Auch hierbei liegt meist eine isolierte Ferritin-Erhöhung vor, ohne dass das Serum-Eisen gleichzeitig erhöht
und das Transferrin erniedrigt ist, was bei den systemischen Eisenüberladungserkrankungen bereits frühzeitig
der Fall ist. 
Die Frage ist, ob ein chronisch erhöhtes Nahrungseisenangebot auch zu einer gewissen Eisenspeicherung
führen kann. Dabei könnte auch Ethanolkonsum eine Rolle spielen, wodurch bekannternmaßen die
Hepcidinsynthese in der Leber gehemmt würde, sodass mehr Nahrungseisen absorbiert würde (2).
Eigentlich sollte der sogenannte “Mukosa-Block” dies auf Dauer verhindern. Dieser auch in aktuellen
Publikationen häufig zitierte Begriff des „Mukosa-Block“ wurde ursprünglich vor 65 Jahren formuliert, um die
Herunterregulation der intestinalen Eisenabsorption als Reaktion auf eine vorangegangener Eisengabe bei
Versuchstieren zu beschreiben (3). Ob es diesen Effekt beim Menschen überhaupt gibt, ist allerdings eher
fraglich. So funktioniert eine orale Therapie mit täglichen Eisen-Dosis bekanntermaßen gut und der „Mukosa-
Block“ schützt auch keineswegs vor einer akuten Intoxikation durch sehr hohe Eisendosen. So kann eine 
Einnahme von 180–300 mg Fe/kg Körpergewicht tödlich sein. Eine Dosis von 10-20 mg Fe/kg gilt als nicht-
akut-toxisch beim Menschen. 
Zutreffender ist es, von einer „Mukosa_Block-Intelligenz“ zu sprechen, die die Eisenabsorption nach dem
Bedarf an Eisen im Körper reguliert. Mit der Regulation der Hepcidinsynthese kennen wir heute einen
Mechanismus, der für diese Intelligenz verantwortlich ist. In einer aktuellen Arbeit fanden z.B. Roe et al.
retrospektiv in Serum-Proben aus einer Eisenabsorptionsstudie mit 54Fe und 57Fe markierten
Testmahlzeiten, dass interindividuelle Schwankungen in der Eisenabsorption zumindest teilweise mit den
Plasmahepcidin-Spiegeln erklärt werden können (4).
In der Literatur wird heute diskutiert, wie effizient diese „Mukosa-Block-Intelligenz“ beim Menschen wirklich
funktioniert, und ob eine hohe Eisenzufuhr auf Dauer nicht unweigerlich zu einer exzessiven
Eisenspeicherung führen muss (5,6). Als Beispiel wird oft die historisch interessante Bantu-Siderose
angeführt, die durch das tägliche Trinken von großem Mengen traditionell in Eisentöpfen gebrauten Biers in
Nordafrika hervorgerufen wurde. Man hat die zugeführten Mengen an Eisen auf 50-100 mg/Tag kalkuliert, was
häufig zu Leberzirrhose, Diabetes und Herzinfarkten führen kann. Durch Verwendung von Edelstahl- oder
Kunststoffgefäße konnte dieses Problem leicht gelöst werden. Einschränkend muss angeführt werden, dass
Alkohol einen direkten Einfluss auf Eisenabsorption haben kann. Neuere Studien legen auch eine genetische
Ursache der Afrikanischen Siderose nahe, obwohl ein definierter Gendefekt bisher nicht gefunden werden
konnte (7). Aus den Erfahrungen mit der Bantu-Siderose kann man mit einem Sicherheitsfaktor von 2 das
obere Limit für eine Nahrungseisenzufuhr mit 25-50 mg/Tag festlegen.
Im Rahmen von z.B. Eisenfortifizierungsprogrammen zur Eisenmangelprophylaxe wird deshalb immer wieder
vor adversen Effekten gewarnt (8). Besonders gefährdet erscheinen Genträger für die C282Y-Mutation zu sein
(Häufigkeit in der Normalbevölkerung ca. 10 %), da diese etwas vermehrt Eisen aus einer normalen Diät
aufnehmen können. In Studien mit markierten Testmahlzeiten hat man diesen Effekt allerdings bisher nicht
eindeutig nachweisen können. Auch sprechen epidemiologische Erkenntnisse aus vielen Studien über
Hämochromatosepatienten eher dagegen, denn Genträger entwickeln im Laufe des Lebens nur in ganz
wenigen Ausnahmefällen deutlich erhöhte biochemische Parameter einer Eisenüberladung und zeigen so gut
wie nie klinische Symptome einer Hämochromatose (9).
Nach unseren Erfahrungen mit nichtinvasiven Lebereisenmessungen finden sich bei vielen Patienten mit
moderat erhöhten Serum-Ferritinwerten (nicht bei allen) auch eine leichte Lebersiderose. Die Messung des
Lebereisens erklärt in diesen Fällen das erhöhte Ferritin und macht andere Ursache (akute-Phase-Protein)
damit unwahrscheinlich. Man kann mit einer begrenzten Aderlasstherapie (z.B. 5-8 mal 300-500 ml im
Abstand von 2-3 Wochen) abbauen, wodurch dann das Ferritin runter geht. Besonders empfiehlt sich dieser
Therapie in Fällen mit erhöhten Leberindikatorenzymen. Hier wird diskutiert, ob erhöhtes Lebereisen als
Cofaktor bei einer Leberzellschädigung wirken kann. 
Eisenüberladung durch orale Eisentherapie? 
Bei therapeutischen Dosen einer oralen Eisentherapie (50-100 mg Fe/Einzeldosis) werden 5-20 % absorbiert.
80-95 % verbleiben längere Zeit im Darmlumen und können dort Auslöser vielerlei Reaktionen werden.
Abhängig von Einzel- und Tagesdosis (> 50-100 mg/Tag), äußert sich dies bei Patienten in den typischen
Eisennebenwirkungen wie Übelkeit, Krämpfe, Schmerzen, Durchfall, Verstopfung. Eine zweite Art von
Nebenwirkung, vom Patienten meist nicht direkt bemerkt, in vermehrtem oxidativen Stress in entzündlichen
Darmgewebe bei M-. Crohn und Colitis Ulcerosa (10). Ein Zusammenhang zwischen einer
Eisensupplementation und dem Risiko für Darmkrebs ist unklar und sehr umstritten.
Eine dritte Art von chronischer adverser Reaktion bei einer langandauernden Eisensupplementation ist die
Ausbildung einer sekundären Eisenüberladung: Ingesamt scheint dies nicht häufig vorzukommen, es gibt dazu
nur Einzelfallberichte (11). Bis 1996 war nicht klar, ob es sich dabei um Fälle einer unentdeckten hereditären
Hämochromatose handeln könnte. Barton et al. beschrieben 2006 vier Fälle, bei den explizit auch auf
genetische Veränderung (HAMP, HFE, TfR2, FPN1, HJV, ALAS2) untersucht wurde (12). In allen Fällen wurde
wegen unklarer oder angeblicher Anämie über viele Jahre (7-61 Jahre!) täglich Eisen oral zugeführt (60-220
mg Fe/Tag). Ein Fall mit ß-Thalassämia minor und homozygoter C282Y-Mutation (Selbstmedikation mit 60 mg
Fe/Tag über 7 Jahre) entwickelte dabei eine schwere Eisenüberladung, Diabetes, Leberzirrhose und 
Herzrhythmusstörungen, und musste später mit 160 Aderlässen behandelt werden. Die anderen Fälle hatten
deutlich mehr Eisen (547-4898 g) über längere Zeit (15-61 Jahre) eingenommen, zeigten auch hohe
Ferritinwerte (ca. 2000 µg/l), bildeten aber keine hämochromatose-typische klinische Symptomatik aus. Der
Grad der Eisenüberladung, erkennbar an der Zahl der notwendigen Aderlässe, korrelierte nicht mit der Dauer
und Menge der Eiseneinnahme.
Diese Fälle zeigen, dass eine nichtindizierte orale Eisentherapie zu einer Eisenüberladung führen kann, die im
Einzelfall auch eiseninduzierte Organschäden auslösen kann. Nur Patienten mit einem dokumentierten
Eisenmangel sollte daher kontrolliert und über eine begrenzte Zeit Eisen einnehmen.
Eisenüberladung durch parenterale Eisentherapie? 
Bei der Behandlung von Eisenmangel-Patienten findet z.Zt. eine Renaissance der parenteralen Eisentherapie
statt. Es handelt sich dabei um kolloidale Fe(III)- Kohlenhydrat- Nanopartikel, die vorzugsweise i.v. appliziert
werden. Da bei i.v.-Injektion von hochmolekularen Eisenverbindungen die „Mukosa-Block-Intelligenz“
naturgemäß außer Kraft gesetzt ist, kann es bei wiederholter Anwendung, wie z.B. bei Patienten mit renaler
Anämie unter Epo-Therapie heute durchaus üblich ist, zu einer Eisenüberladung kommen
Makrophagen sind an der Plasmaclearance der i.v. applizierten hochmolekularen Substanzen wesentlich
beteiligt, wobei der Metabolismus der jeweiligen Verbindung sehr von der Größe und der Hülle der kolloidalen
Nanopartikel abhängig ist. Dabei wird offenbar nicht die ganze Substanz restlos metabolisiert und der
Erythropoese zur Verfügung gestellt, sondern ein Teil wird z.B. in langlebigen Zellen in Leber und
Knochenmark gespeichert Diese „residuelle Endothelsiderose“ (Hausmann) bleibt auch in Gegenwart einer
Eisenmangelanämie bestehen, was zeigt, dass es sich hierbei um schwer mobilisierbares Eisen handelt (13).
Es ist schon lange bekannt, dass man bei einer histologischen Begutachtung von Knochenmarkspunktaten
denjenigen Patienten leicht identifizieren kann, der in der Vorgeschichte jemals eine Injektion mit bestimmten
Eisenverbindungen erhalten hat. Es wurde deshalb früher von der leichtfertigen Anwendung einer
parenteralen Eisentherapie immer wieder gewarnt (14, 15). Diese Erkenntnis einer Eisenspeicherung nach i.v.
Eisengabe wird gerade wieder neu entdeckt (16). Diese gleiche Problematik ergibt sich heute auch durch die
Anwendung von eisenbasierten Nanopartikeln in der MRI-Kontrastgebung (z.B. „molekulares Imaging“). Von
zugelassenen Präparaten wie Endorem® oder Resovist® ist diesbezüglich auch sehr wenig bekannt, obwohl
teilweise hohe
Literatur2. Costa-Matos L, Batista P, Monteiro N, Simões M, Egas C, Pereira J, Pinho H, Santos N, Ribeiro J, Cipriano MA, Henriques P,
Girão F, Rodrigues A, Carvalho A. Liver hepcidin mRNA expression is inappropriately low in alcoholic patients compared with
healthy controls. Eur J Gastroenterol Hepatol. 2012 Oct;24(10):1158-65. doi: 10.1097/MEG.0b013e328355cfd0.
4. Hahn PF, Bale WF. Ross IF, Balfour WM, Whipple GH. Radioactive iron absorption by gastro-intestinal tract: influence of
anemia, anoxia, and antecedent feeding. J Exp Med 1943; 78:169-88
5. Roe MA, Heath AM, Oyston SL, Macrow C, Hoogewerff JA, Foxall R, Dainty JR, Majsak-Newman G, Willis G, Fairweather-Tait
SJ. Iron absorption in male C282Y heterozygotes. Am J Clin Nutr 2005;81:814 –21
6. Salonen JT, Nyyssonen K, Korpela H, Tuomilehto. J,. Seppanen. R,. Salonen R. High stored iron levels are associated with
excess risk of myocardial infarction in eastern Finnish men. Circulation 1992; 86(3):803-11
7.
Gordeuk VR, Mukiibi J, Hasstedt SJ, Samowitz W, Edwards CQ, West G, Ndambire S, Emmanual J, Nkanza N,
Chapanduka Z, Randall M, Boone P, Romano P, Martell RW, Yamashita T, Effler P, Brittenham G. Iron overload in Afrika.
Interaction between a gene and dietary iron content. N Engl J Med 1992; 326:95-100
8.
Schümann K, Ettleb T, Szegnera B, Elsenhans B, Solomons NW. On risks and benefits of iron supplementation
recommendations for iron intake revisited. J Trace Elem Med Biol 2007; 21:147–168
9. Singh M, Ashwell M, Sanderson P, Cade J, Moreton J, Fairweather-Tait S, Roe M, Marx JJ, Worwood M, Cook JD. Risk of
iron overload in carriers of genetic mutations associated with hereditary haemochromatosis: UK Food Standards Agency
workshop. Br J Nutr 2006; 96(4):770-3
10.
Erichsen K, Ulvik RJ, Nysaeter G, Johansen J, Ostborg J, Berstad A, Berge RK, Hausken T. Oral ferrous fumarate or
intravenous iron sucrose for patients with inflammatory bowel disease. Scand J Gastroenterol. 2005;40(9):1058-65
11.
Green P, Eviatar JM, Sirota P, Avidor I.Secondary hemochromatosis due to prolonged iron ingestion. Isr J Med Sci.
1989; 25(4):199-201
12.
Barton JC, Lee PL, West C, Bottomley SS.Iron overload and prolonged ingestion of iron supplements: clinical features
and mutation analysis of hemochromatosis-associated genes in four cases. Am J Hematol. 2006; 81(10):760-7
13
Hausmann K, Wulfhekel U, Diillmann J, Kuse R. Iron Storage in Macrophages and Endothelial Cells. Histochemistry,
Ultrastructure, and Clinical Significance. Blut 1976; 32: 289-295.
14.
Fishbane S. Intravenous iron therapy: reweighing risk and reward. Semin Dialysis. 1999;12:5-8.
15. Besarab A, Frinak S, Yee J: An indistinct balance: the safety and efficacy of parenteral iron therapy. J Am Soc Nephrol
1999, 10:2029-2043.
16. Thomason RW, Almiski MS. Evidence that stainable bone marrow iron following parenteral iron therapy does not correlate
with serum iron studies and may not represent readily available storage iron. Am J Clin Pathol. 2009 Apr;131(4):580-5. Links











© www.eiseninfo.de
unklar erhöhtes Ferritin
Serum-Ferritin als Laborparameter gibt es seit ca. 1970.
Es wird offenbar von Leberzellen und anderen (?) Zellen
gebildet und ins Blut abgegeben und zeigt dabei die
Eisenspeicherung in diesen Zellen an.
Das Serum-Ferritin ist als diagnostischer Parameter für
Eisenmangel und Eisenüberladung wichtig. Im
Eisenmangel zeigt es die Entleerung der Eisenspeicher
an. Werte < 12 µg/l bedeuten vollkommen erschöpfte
Eisenspeicher. Das Schöne ist, es gibt keine falsch
erniedrigten Serum-Ferritinwerte und es gibt auch keine
Tag-zu-Tag-Variation. Bei Eisenüberladung (Hämo-
chromatose, Transfusions-bedingter Hämosiderose)
steigt der Ferritinwert an und erlaubt auch eine
Abschätzung der erhöhten Eisenspeicher, wobei hier
große individuelle Variaten gibt (besser ==> Lebereisen).
Es gibt aber viele Patienten, die keine genetische
Eisenspeicherkrankheit haben und trotzdem erhöhte 
Ferritinwerte aufweisen. Es gibt damit also relativ häufig
falsch erhöhte Ferritinwerte. 

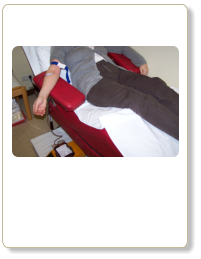
Eisenüberladung
Aderlasstherapie. Methode aus dem Mittelalter!? Für Eisenspeicherkrankheit aber hochmodern